1. 서론
2. 재료 및 방법
3. 결과
3.1 잘피 서식지 면적 및 종조성
3.2 잘피 밀도 및 전장
4. 고찰
1. 서론
잘피는 수생 현화식물로 뿌리, 줄기, 잎으로 구분되어 있고 수중에서 꽃을 피우고 씨를 맺는 해초류(seagrass)이다(Den Hartog 1970). 전 세계적으로 5과 13속 60여 종이 서식하며, 우리나라는 4속 9종의 서식이 기록되어 있다(Short et al. 2001; Kim et al. 2009). 잘피 서식지 면적은 1970년대 이전 55-70 km2 정도로 추정되었으나, 이후 산업화에 따른 연안역의 무분별한 개발과 굴, 해조류 양식장 시설의 증가 등 다양한 인간 활동의 영향으로 인해 서식지 감소가 급격하게 진행되고 있는 것으로 밝혀져 있다(Lee and Lee 2003). 잘피숲은 해양의 1차 생산자일 뿐만 아니라, 다양한 해양생물의 산란장, 기질 및 은신처이며, 치어들에게 피난처가 되는 보육장의 역할을 하기도 함으로써 해양생태계의 생물다양성을 유지하는 역할을 한다. 이들이 뿌리와 잎을 통해 퇴적물과 해수 중의 영양염을 흡수하여 높은 수질정화의 기능도 가진다는 사실은 이미 오래전부터 보고되어 왔다(Johnstone 1978; Fonseca et al. 1996; Thomas and Cornelisen 2003; Park et al. 2020). 또한 잘피숲은 해양생태계 중 기초생산력이 매우 높은 지역으로, 순일차생산량(NPP)은 맹그로브숲 다음으로 높다고 알려져 있다(Duarte and Cebrián 1996; Duarte and Chiscano 1999). 이러한 잘피의 생태학적 역할이 확인되면서 잘피 서식지 보호·보전 및 복원과 관련된 많은 연구가 진행 중이며(Paling et al. 2001; Lee and Park 2008; Li and Lee 2010; Park et al. 2011), 최근에는 「해양생태계의 보전 및 관리에 관한 법률」에 따른 해양 보호 생물로 6종(Zostera marina, Z. caulescens, Z. asiatica, Z. caespitosa, Phyllospadix japonicus, P. iwatensis)이 지정되어 관리되고 있다.
육상과 달리 수생생물 조사는 여러 가지 제한요인으로 인해 어려움이 따른다. 수생생물의 조사방법은 전통적으로 SCUBA diving을 이용한 잠수 조사가 주를 이루었으나, 최근에는 수중음향, 드론을 이용한 항공촬영, 인공위성을 이용한 조사 등 새로운 연구 방법들이 계속적으로 적용되고 있다(Kang et al. 2006; Kim et al. 2015; Jeon et al. 2020). 하지만 이러한 원거리 조사 방법은 넓은 면적의 분포 현황을 파악할 때는 효과적일 수 있으나, 조사 환경에 따른 결과 차이가 발생할 수 있기 때문에 정확한 결과를 얻기 위해서는 근거리 조사 방법을 병행하는 것이 필요하다.
최근 빠른 속도로 진행되고 있는 지구온난화는 수온 상승과 같은 해양환경의 변화를 일으키고 이는 동해에서 한류성 어종의 감소와 난류성·아열대성 어종의 증가, 갯녹음 증가와 해파리와 같은 유해종의 대량 번식 등 해양 생태계에 다양한 영향을 미치는 것으로 확인되고 있으며(Kim 2010), 이러한 변화를 예측하고 관리하기 위해서는 해양 생태계에 대한 지속적인 관찰이 필요하다. 잘피 서식지와 같이 환경 영향으로 인한 질적·양적 변화가 이미 진행 중인 생태계는 장기적인 관점에서 모니터링 연구를 통해 군락의 변화 과정을 이해하고, 군락의 변화를 유발하는 주된 요인을 파악하여 관리하는 것이 중요하다. 전남 해안과 다도해역은 우리나라 남서쪽에 위치해 있으며 전국에서 가장 많은 섬(전국 도서의 약 60%)과 긴 해안선(전국 해안선의 약 50%)을 가지고 있다. 이 해역은 비교적 얕은 수심을 가지며 반일주조가 우세하고 육상기원 쇄설물의 유입이 많아 조류 및 파랑의 영향으로 퇴적물의 재부유로 인한 연중 탁한 해수를 나타내는 해역이다(Choo and Kim 2013; Choo and Kim 2018).
이 연구는 최근 해수온 상승 등 전 지구적인 변화와 인간의 연안 활동 등에 의한 인위적인 교란을 포함하는 다양한 환경변화에 따라 서식면적이 감소하고 출현 개체수가 줄어들고 있는 잘피 군락을 대상으로, 전남 해안 및 다도해역 잘피 서식지의 면적, 해역별 종조성, 개체 밀도, 형태 등을 파악하여 대상 해역에 자생하는 잘피의 분포 특성과 생태적 특징을 분석하고 추후에 활용 가능한 기본적인 자료 구축을 목적으로 진행하였다.
2. 재료 및 방법
전남 해안 및 다도해역의 잘피 서식지 연구를 위해 일차적으로 문헌 조사와 어촌계 탐문 조사를 실시한 후 잘피 서식이 확인된 지역을 대상으로 현장 조사를 수행하였다(Fig. 1). 현장 조사는 드론(MAVIC 2 PRO, DJI, Korea)으로 항공촬영을 실시하여 잘피 서식지 분포 확인한 후 DPV(diver propulsion vehicle)와 SCUBA diving을 이용한 잠수 조사로 잘피 출현종을 확인하였다. 잠수 조사자는 수면에 노출된 GPS를 끈으로 연결하여 수중에서 조사자의 이동 좌표를 획득하였고, 이를 항공사진과 병행하여 잘피 군락 면적을 산출하였다.
잠수 조사 시 잘피 서식 밀도 분석을 위해 25 × 25 cm ‘ㄷ’자형 방형구를 이용하여 방형구 내 개체수를 계수하였고, 4회 반복 조사하여 단위면적 당 개체수(shoot m-2)로 환산하였다. 또한 수중에서 잘피 4개체를 대상으로 지상부 전장을 측정하였다.
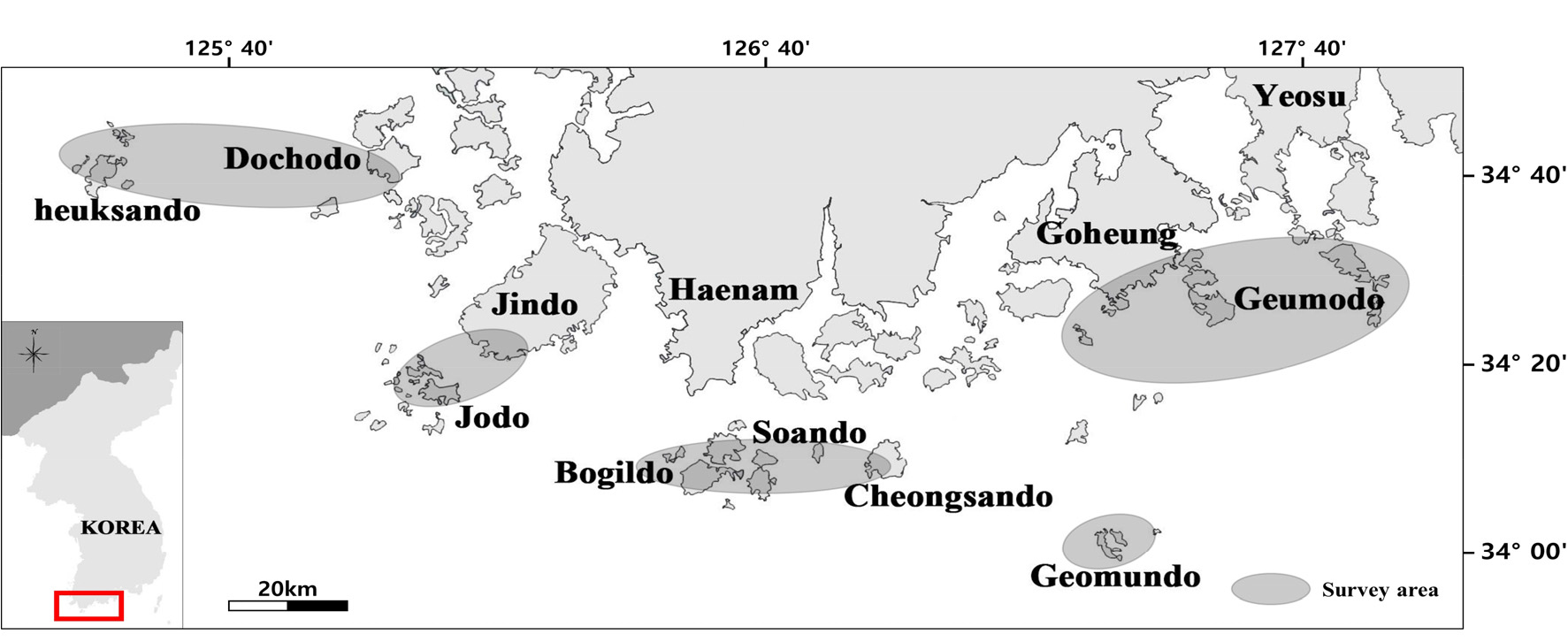
Fig. 1
A map showing location of survey area of Korea.
3. 결과
3.1 잘피 서식지 면적 및 종조성
이 연구를 통해 전남 해안 및 다도해역에서 출현한 잘피는 거머리말(Zostera marina), 수거머리말(Z. caulescens), 포기거머리말(Z. caespitosa), 애기거머리말(Z. japonica), 새우말(Phyllospadix iwatensis), 해호말(Halophila nipponica) 등 6종이 확인되었다. 잘피 서식지는 새우말이 확인된 거문도 덕촌리와 대장도를 제외하면 파도의 영향을 덜 받는 조용한 내만에 위치하고 있었으며, 기질은 대부분 니질이었다. 이 연구에서 확인된 잘피 서식지 면적은 총 4,412,944 m2이며, 조사해역 중 가장 넓은 면적은 소안도 비자리 해역으로 약 1,977,698 m2로 나타났다. 출현종별 서식면적은 거머리말 4,324,894 m2 (97.1%), 수거머리말 70,248 m2 (1.6%), 애기거머리말 45,180 m2 (1.0%), 해호말 10,721 m2 (0.2%), 새우말 1,105 m2 (0.1%이하), 포기거머리말 350 m2 (0.1%이하)순으로 나타났다(Fig. 2). 출현종별 생육수심은 거머리말 1.0~4.5 m, 수거머리말 1.5~4.6 m, 포기거머리말 2.0~3.5 m, 새우말 2.5~3.0 m, 해호말 4.0 m 등의 범위에서 생육하였으며, 애기거머리말은 조간대에서만 확인되었다.

Fig. 2
Distribution area of seagrass habitat using drones. 1:Ando Ayaman, 2:Geumodo Usilpo, 3:Geumodo Uhak-ri, 4:Hwataedo Myodu, 5:Hwataedo Hwatae-ri, 6:Hwataedo Dokjeong, 7:Narodo Changpo, 8:Narodo Beach, 9:Narodo Sangcho, 10:Jijukdo, 11:Geomundo Dongdo-ri, 12:Geomundo Seodo-ri, 13:Geomundo Deokchon-ri, 14:Soando Iwol-ri, 15:Soando Bija-ri, 16:Bogildo Jungtong-ri, 17:Bogildo Deungmun, 18:Bogildo Jeongja-ri, 19:Cheongsando Dangrak-ri, 20:Cheongsando Docheong-ri, 21:Sangjodo Dangdo-ri, 22:Sangjodo Yeomi-ri, 23:Sangjodo Yulmok Harbor, 24:Nabaedo, 25:Hajodo Changyu-ri, 26:Hajodo Sinjeon Beach, 27:Jindo Namdong-ri, 28:Dochodo Simok Beach, 29:Daejangdo, 30:Damuldo, 31:Daedundo Su-ri, 32:Daedundo O-ri, 33:Yeongsando, 34:Heuksando Jin-ri, 35:Heuksando Baenanggimi.
3.2 잘피 밀도 및 전장
거머리말의 밀도와 전장은 연구 해역과 출현종에 따라 차이를 보였는데, 밀도는 거문도 서도리에서 252±15.3 shoot m-2로 가장 높았고, 나로도해수욕장에서 44±8.0 shoot m-2로 가장 낮았다. 수거머리말의 밀도는 보길도 중통리에서 124±8.0 shoot m-2로 가장 높았고, 다물도 수리에서 20±8.0 shoot m-2로 가장 낮았다. 거머리말의 전장은 전체 평균 115.4±25.3 cm이며, 보길도 등문에서 158.3±16.6 cm로 가장 길었고, 거문도 동도리에서 65.3±7.4 cm로 가장 짧았다. 수거머리말의 전장은 전체 평균 210.6±38.2 cm로 거머리말과 약 1 m의 차이를 보였는데, 보길도 중통리에서 291.8±8.5 cm로 가장 길었고, 대둔도 수리에서 172.3±11.4 cm로 가장 짧았다(Table 1).
Table 1.
Individual characteristics of seagrass at study sites.
|
Site
|
Species
|
Area (m2)
|
Depth(m)
|
Shoot density
(shoots m-2)
|
Length of plants
(cm)
|
|
Ando Ayaman
| Z. marina |
10,721
|
4
|
140± 24
|
81.3±8.7
|
| H. nipponica |
1,064±125.6
|
3.0±0.0
|
|
Geumodo Usilpo
| Z. marina |
470
|
2
|
176±18.5
|
137.5±8.7
|
|
Geumodo Uhak-ri
| Z. marina |
10,068
|
2.4
|
168±9.2
|
126.5±6.5
|
|
Hwataedo Myodu
| Z. marina |
37,095
|
2
|
132±30.3
|
128.5±8.3
|
|
Hwataedo Hwatae-ri
| Z. marina |
11,333
|
2
|
104±9.2
|
121.0±7.0
|
|
Hwataedo Dokjeong
| Z. marina |
869
|
2
|
116±8.0
|
125.5±9.9
|
|
Narodo Changpo
| Z. marina |
75,785
|
1.3
|
84±15.3
|
109±10.7
|
|
Narodo Beach
| Z. marina |
86,745
|
0.7
|
44±8.0
|
67.3±4.1
|
| Z. japonica |
28,910
|
intertidal
|
2,112±0.0
|
33±2.7
|
|
Narodo Sangcho
| Z. marina |
133,643
|
1
|
92±15.3
|
96±6.8
|
|
Jijukdo
| Z. marina |
6702
|
1.5
|
88±20.7
|
114.8±5.7
|
|
Geomundo Dongdo-ri
| Z. marina |
27,646
|
4.5
|
172±20.1
|
65.3±7.4
|
|
Geomundo Seodo-ri
| Z. marina |
48,005
|
4.3
|
252±15.3
|
82±5.8
|
|
Geomundo Deokchon-ri
| P. iwatensis |
-
|
3
|
2,025±44.1
|
72.3±6.4
|
|
Soando Iwol-ri
| Z. marina |
662,660
|
2
|
116±27.3
|
154±9.0
|
|
Soando Bija-ri
| Z. marina |
1,977,698
|
1
|
160±13.1
|
142.3±13.6
|
|
Bogildo Jungtong-ri
| Z. marina |
667,968
|
2
|
160±13.1
|
154.8±17.6
|
| Z. caulescens |
7,954
|
3
|
124±8.0
|
291.8±8.5
|
|
Bogildo Deungmun
| Z. marina |
54,828
|
2
|
164±15.3
|
158.3±16.6
|
|
Bogildo Jeongja-ri
| Z. marina |
25,666
|
2.5
|
156±15.3
|
144.5±12.7
|
|
Cheongsando Dangrak-ri
| Z. marina |
941
|
2.8
|
136±27.7
|
114±15.1
|
|
Cheongsando Docheong-ri
| Z. caulescens |
16,761
|
4.6
|
88±20.7
|
192.8±13.3
|
| Z. marina |
29,194
|
2.5
|
140±15.3
|
127.5±8.3
|
|
Sangjodo Dangdo-ri
| Z. marina |
213,537
|
1~2
|
140±15.3
|
102.8±11.5
|
| Z. japonica |
50
|
intertidal
|
336±67.9
|
13.5±1.3
|
|
Sangjodo Yeomi-ri
| Z. marina |
128
|
2
|
104±9.2
|
93.5±8.0
|
|
Sangjodo Yulmok Harbor
| Z. marina |
36,364
|
2.5
|
136±9.2
|
112.3±10.2
|
| Z. japonica |
13,646
|
intertidal
|
1,280±136.6
|
12.3±1.3
|
|
Nabaedo
| Z. marina |
104,768
|
2
|
140±8.0
|
119.3±17.7
|
|
Hajodo Changyu-ri
| Z. marina |
17,209
|
1~1.5
|
96±13.1
|
100.3±14.9
|
| Z. caulescens |
100
|
2.5
|
88±9.2
|
179.3±11.9
|
|
Hajodo Sinjeon Beach
| Z. marina |
780
|
2
|
96±13.1
|
119.8±20.6
|
|
Jindo Namdong-ri
| Z. marina |
2,583
|
2
|
52±8.0
|
123.3±15.2
|
| Z. caulescens |
3
|
60±8.0
|
182.5±13.2
|
|
Dochodo Simok Beach
| Z. marina |
16,012
|
1
|
92±8.0
|
83.5±10.8
|
| Z. caulescens |
9,257
|
1.5~2.5
|
104±9.2
|
219.5±17.5
|
|
Daejangdo
| P. iwatensis |
1,105
|
2.5
|
2,100±57.5
|
99.8±7.5
|
|
Damuldo
| Z. marina |
21,846
|
1~2
|
136±20.7
|
119.8±7.4
|
| Z. japonica |
2,574
|
intertidal
|
1,920±229.6
|
16.5±2.4
|
|
Daedundo Su-ri
| Z. marina |
1,204
|
2
|
96±13.1
|
128±12.6
|
| Z. caulescens |
223
|
4.5
|
20±8.0
|
172.3±11.4
|
| Z. caespitosa |
350
|
2~3.5
|
30±0.0
|
69.5±7.4
|
|
Daedundo O-ri
| Z. marina |
1,215
|
3
|
116±15.3
|
123.5±11.3
|
| Z. caulescens |
202
|
4
|
100±15.2
|
201.5±13.3
|
|
Yeongsando
| Z. marina |
3,022
|
2.5
|
152±20.7
|
69.5±9.6
|
| Z. caulescens |
708
|
4
|
108±15.3
|
261.3±17.4
|
|
Heuksando Jin-ri
| Z. marina |
11,939
|
3.5
|
144±13.1
|
113.5±15.9
|
| Z. caulescens |
6,210
|
4
|
136±9.2
|
193.8±12.3
|
|
Heuksando Baenanggimi
| Z. marina |
26,250
|
3
|
176±13.1
|
148.5±17.3
|
| Z. caulescens |
3.5
|
148±8.0
|
211.3±11.0
|
4. 고찰
이 연구에서 전남 해안 및 다도해역에서 자생하는 잘피는 총 6종이 확인되었다. 우리나라 연안에 자생하는 잘피 중 대부분을 차지하는 거머리말은 조용한 내만의 연성기질에 서식하며 해양생태계 내에서 서식처, 산란장, 보육장, 은둔처 및 생활기반의 제공 등 중요한 생태적 역할을 담당한다고 알려져 있다(Park et al. 2020). 거머리말은 이 연구에서 조사된 면적의 약 97%를 차지할 정도로 넓은 면적에 서식하고 있었으며, 내만 또는 섬과 섬 사이에서 밀생하여 서식하였다. 하지만 이전 연구 결과(Ahn et al. 2015) 중 동일 지역의 밀도 자료를 비교하였을 때, 대부분의 지역에서 생육 밀도가 낮아진 것으로 확인되었다(Table 2). 많은 지역에서 잘피류의 서식 밀도가 감소한 결과는 현재로선 명확한 원인을 제시하기 어려우며, 환경 오염, 해안개발, 생활 오폐수 유입, 매립 및 간척 사업 등 다양한 원인이 있을 것으로 추정된다. 이 연구 해역의 감소 원인을 밝히기 위해서는 장기적인 관점에서 지속적이며 추가적인 모니터링과 함께 환경요인 조사를 병행한 통합적인 조사가 수행되어야 할 필요가 있을 것으로 판단된다.
Table 2.
Comparison of shoot density between previous and this studies at the same site (Unit: shoot m-2).
|
Reference
|
Geomundo
|
Soando
|
Damuldo
|
Heuksando
|
Dochodo
|
| Ahn et al. (2015) |
333.33
|
319.87
|
266.67
|
214.40
|
261.50
|
|
This study
|
212.00
|
138.00
|
136.00
|
176.00
|
92.00
|
애기거머리말은 주로 조간대에 서식하는 종으로 해양수산부에서 법령화 한 해양보호생물로 지정되어 있지는 않지만, 거머리말속의 다른 잘피류에 비해 서식 환경과 조건이 매우 취약한 편으로, 조간대에 생육한다는 서식 특성상 인간 활동에 의한 인위적인 교란과 서식지 환경 변화, 해양 환경 변화 등으로 인해 서식지가 파괴되기 쉬운 것으로 알려져 있다(Lee et al. 2004). 실제로 과거 거제도 다대 해역 조간대에 애기거머리말 군락이 존재하였으나(Lee et al. 2006) 주변이 갯벌 체험장소로 사용되면서 애기거머리말이 사라졌는데, 이는 잘피 서식지 파괴 사례 중 하나이다. 이 연구에서 애기거머리말의 서식지들은 소규모 면적이었지만 과거에 비해 대부분 높은 생육 밀도를 나타냈다. 하지만 나로도해수욕장의 경우 관광객의 출입이 자유로워 이로 인한 생태계 교란이 예상되어 별도의 잘피 서식지 보호 조치를 취할 필요가 있을 것으로 판단된다.
유엔기후변화협약 제22차 당사국회의에서 「해양과 기후에 관한 전략행동 로드맵(Strategic Action Roadmap on Oceans and Climate : 2016 to 2021)」이 채택됨으로서 해양부문 탄소흡수원으로 잘피 연구가 활발히 이루어지고 있다(Thorhaug et al. 2017; Stankovic et al. 2021). 잘피는 육상산림의 약 1.4배 높은 탄소 고정량을 보유한다고 연구되었지만(Kim et al. 2008) 산림에 비해 좁은 서식 면적 때문에 상대적으로 낮은 평가를 받아왔고, 그 중요성도 심각하게 고려되지 않은 측면이 있다. 이 연구에서 확인된 잘피 서식지는 약 4.4 km2로 분석되었지만, 과거 동일지역에 대한 서식지 면적의 규모에 대한 조사 기록이 없어 직접 비교는 불가능하였다. 그러나, 현장 연구 해역 주변에서 실시한 어업인 대상의 탐문조사를 통하여 대부분 어촌계에서 과거에 비해 서식지가 상당 부분 소실된 것을 확인할 수 있었다. 이러한 원인을 규명하기 위한 첫 번째 단계가 장기적인 관점에서 지속적인 모니터링을 통한 잘피 군락의 분포 현황을 확인하고, 잘피 서식지의 생물·물리·화학적 환경변화를 파악하는 것이라고 판단된다. 지구온난화에 따른 한반도 주변 수온 상승을 포함한 다양한 환경변화에 대응하기 위해서 이들의 생태학적 기능 및 역할과 함께 환경변화에 따른 잘피 군락의 변동양상에 대한 추가적인 관찰과 연구가 지속적으로 수행되어야 할 것이다.
Acknowledgements
이 연구는 「2021년 다도해해상국립공원 공원자원조사 해양생태계 분야(조간대 해양생태계)」 사업으로 수행되었습니다.
References
Ahn JK, Jeong JB and Kim CD. 2015. Seagrasses of Dadohaehaesang National Park, Korea in 2014. Journal of National Park Research 6, 163-168.
Choo HS and Kim DS. 2013. Tide and tidal currents around the archipelago on the southwestern waters of the south sea, Korea. Journal of the Korean Society of Marine Environment & Safety 19, 582-596.
10.7837/kosomes.2013.19.6.582.Choo HS and Kim DS. 2018. Characteristics of tidal current and tidal residual current in the archipelago around aphae island in the southwestern waters of Korea. Journal of the Korean Society of Marine Environment & Safety 24, 179-187.
10.7837/kosomes.2018.24.2.179.Den Hartog C. 1970. The seagrass of the world. North Holland Publishing Company, Amsterdams, London. 275 pp.
Duarte CM and Cebrián J. 1996. The fate of marine autotrophic production. Limnol. Oceanogr. 41, 1758-1766.
10.4319/lo.1996.41.8.1758.Duarte CM, Chiscano CL. 1999. Seagrass biomass and production: a reassessment. Aquatic Botany 65, 159-174.
10.1016/S0304-3770(99)00038-8.Fonseca MS, Meyer DL and Hall MO. 1996. Development of planted seagrass beds in Tampa Bay, Florida, USA. Ⅰ. Plant components. Mar Ecol Prog Ser 132, 128-139.
10.3354/meps132127Jeon EI, Kim SH, Kim BS, Park KH and Choi OI. 2020. Semantic segmentation of drone imagery using deep learning for seagrass habitat monitoring. Korean Journal of Remote Sensing 36, 199-215.
10.7780/kjrs.2020.36.2.1.8.Johnstone IM. 1978. The ecology and distribution of Papua New Guinea seagrasses. II. The Fly Islands and Raboin Island. Aquatic Botany. 5, 235-243.
10.1016/0304-3770(78)90066-9.Kang DH, Cho SH, La HS, Kim JM, Na JY and Myoung JG. 2006. Estimating spatial and vertical distribution of seagrass habitats using hydroacoustic system. Ocean and polar research 28, 225-236.
10.4217/OPR.2006.28.3.225.Kim DH. 2010. Global warming effect on marine environments and measure practices against global warming. Korean Soc. Mar. Environ. Saf. 16, 421-425.
Kim JB, Park JI and Lee KS. 2009. Seagrass Distribution in Deukryang Bay. Kor. J. Fish Aquat. Sci. 42, 509-517.
10.5657/kfas.2009.42.5.509.Kim JB, Park JI, Jung CS, Lee PY and Lee KS. 2009. Distributional range extension of the seagrass
Halophila nipponica into coastal waters off the Korean peninsula. Aquatic Botany 90, 267-272.
10.1016/j.aquabot.2008.10.007.Kim KY, Choi JK, Ryu JH, Jeong HJ, Lee KT, Park MG and Kim KY. 2015. Observation of typhoon-induced seagrass die-off using remote sensing. Estuarine, Coastal and Shelf Science 157. 111-121.
10.1016/j.ecss.2014.12.036.Kim TH, Park SR, Kim YK, Kim JH, Kim SH, Kim JH, Chung IK and Lee KS. 2008. Growth dynamics and carbon incorporation of the seagrass,
Zostera marina L. in Jindong Bay and Gamak Bay on the southern coast of Korea. Algae 23, 241-250.
10.4490/ALGAE.2008.23.3.241.Lee KS and Lee SY. 2003. The seagrasses of the republic of Korea. In:World Atlas of Seagrasses: present status and future conservation. Green CP, Short FT and Spalding MD, eds, University of California Press, Berkeley, U.S.A., 193-198.
Lee KS and Park JI. 2008. An effective transplanting technique using shells for restoration of
Zostera marina habitats. Mar. Pollut. Bull. 56, 1015-1021.
10.1016/j.marpolbul.2008.02.01018342894Lee SH, Ma SM, Lim YS, Choi HK and Shin HC. 2004. Genetic Diversity and Its Implications in the Conservation of Endangered
Zostera japonica in Korea. Journal of Plant Biology 47, 275-281.
10.1007/BF03030519.Lee SY, Kim JB and Lee SM. 2006. Temporal dynamics of subtidal
Zostera marina and intertidal
Zostera japonica on the southern coast of Korea. Marine Ecology 27, 133-144.
10.1111/j.1439-0485.2006.00089.x.Li WT and Lee KS. 2010. Adaption success of
Zostera marina to a new transplant environment. Algae 25, 27-35.
10.4490/algae.2010.25.1.027.Paling EI, Keulen MV, Wheeler K, Phillips J and Dyhrberg R. 2001. Mechanical seagrass transplantation in Western Australia. Ecological Engineering 16, 331-339.
10.1016/S0925-8574(00)00119-1.Park JI, Kim JH, Song HJ and Kim GY. 2020. Distribution of the Seagrass,
Zostera spp. in Ulleungdo. J. Korean Soc. Oceanogr. 25, 106-116.
10.7850/jkso.2020.25.4.106.Park JI, Lee KS and Son MH. 2011. Growth Dynamics of
Zostera marina Transplants in the Nakdong Estuary Related to Environmental Changes. Korean Journal of Fisheries and Aquatic Sciences 44, 533-542.
10.5657/kfas.2011.0533.Short FT, Coles RG and Christine PM. 2001. Global Seagrass Research Method. In: Global seagrass distribution. Frederick T. Short, Robert G. Coles, Catherine A. Short, eds, Elsevier, 5-31.
10.1016/B978-044450891-1/50002-5Stankovic M, Ambo-Rappe R, Carly F, Dangan-Galon F, Fortes MD, Hossain MS, Kiswara W, Van Luong C, Minh-Thu P, Mishra AK, Noiraksar T, Nurdin N, Panyawai J, Rattanachot E, Rozaimi M, Soe Htun U and Prathep A. 2021. Quantification of blue carbon in seagrass ecosystems of southeast asia and their potential for climate change mitigation. Sci. Total Environ. 783, 146858.
10.1016/j.scitotenv.2021.146858.Thomas FI and Cornelisen CD. 2003. Ammonium uptake by seagrass communities:effects of oscillatory versus unidirectional flow. Marine Ecology Progress Series 247, 51-57.https://doi.org/10.3354/meps247051
10.3354/meps247051Thorhaug A, Poulos HM, López-Portillo J, Ku TC and Berlyn GP. 2017. Seagrass blue carbon dynamics in the Gulf of Mexico: Stocks, losses from anthropogenic disturbance, and gains through seagrass restoration. Science of The Total Environment 605-606, 626-636.
10.1016/j.scitotenv.2017.06.189.