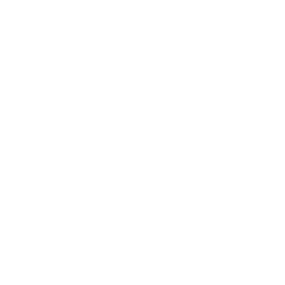1. 서론
2. 재료 및 방법
3. 결과 및 고찰
4. 결론
1. 서론
꼬시래기과(Gracilariaceae)는 분홍치홍조아강(Rhodymeniophycidae), 꼬시래기목(Gracilariales)에 속하는 대표적인 다세포성 홍조식물이다(Verbruggen et al. 2010). 꼬시래기과 홍조류는 식품 및 사료 원료로 활용되고 있으며, 아가(agar), 아가란(agarans)과 다양한 생리활성 화합물추출에 쓰이는 유용성 종을 다수 포함한다(Freile-Pelegrin and Murano 2005; Andriani et al. 2016). 꼬시래기과 홍조류는 전세계에 239종이 분포하며(Guiry and Guiry 2021), 여러 번의 분류학적 개정을 거쳐 현재 2아과 4속(Curdiea속 11종, 꼬시래기속 Gracilaria 200종, 개꼬시래기속 Gracilariopsis 24종 및 Melanthalia속 4종)으로 분류된다(Kim et al. 2008; Gurgel et al. 2018; Lyra et al. 2021). 우리나라의 꼬시래기류는 2속 10종이 알려져 있다: 활꼬시래기(Gracilaria arcuata Zanardini), 덮꼬시래기[G. corticata (J.Agardh) J.Argdh], 쐐기꼴꼬시래기[G. cuneiforlia (Oamura) I.K.Lee & Kurogi], 먹꼬시래기[G. edulis (S.G.Gmelin) Gurgel & Fredericq], 큰꼬시래기(G. gigas Harvey), 꼬불꼬시래기(G. incurvata Okamura), 각시꼬시래기(G. parvispora I.A.Abbott), 잎꼬시래기[G. textorii (Suringar) Hariot], 꼬시래기[G. vermiculophylla (Ohmi) Papenfuss] 및 개꼬시래기[Gracilariopsis chorda (Holmes) Ohmi] (Lee and Kang 2001; Kim et al. 2013; National list of species of Korea 2021).
꼬시래기(Gracilaria vermiculophylla; 기준표본 채집지: 일본 홋카이도 아케시)는 우리나라를 포함한 북서태평양 고유종이며(Ohmi 1956; Yoshida et al. 1995), 지난 30-40년간 북미(캐나다 서부 및 미국 동부), 중남미(멕시코)를 비롯하여 유럽(스페인, 프랑스, 독일, 스웨덴 및 지중해) 등 전세계 곳곳으로 이동한 침입종으로도 잘 알려져 있다(Freshwater et al. 2006; Weinberger et al. 2008; Kim et al. 2010; Sfriso et al. 2012; Hu and Juan 2014; Kueger-Hadfield et al. 2017). 최근까지 꼬시래기의 생태 및 생물지리학적 연구에서는 미토콘드리아 cox1과 같이 변이가 높은 유전자 서열 자료를 주로 사용하였으며(Yang et al. 2008), 이는 본 종의 기원 지역, 유입 지역 및 분산 과정에 대한 정보를 제공하고 있다(Kim et al. 2010; Gulbransen et al. 2012; Nettleton et al. 2013). 유전체 분석이 보편화되면서 꼬시래기류의 미토콘드리아 유전체(Zhang et al. 2012; Campbell et al. 2014; Yang et al. 2014), 색소체 유전체(Campbell et al. 2014; Du et al. 2016; Lee et al. 2016; Ng et al. 2017; Ho et al. 2018), 전사체(Xiang et al. 2022) 및 핵 유전체(Lee et al. 2018; Lyra et al. 2021) 등 다양한 유전체 수준의 연구가 수행되고 있다. 이러한 연구들은 색소체 및 미토콘드리아 유전체 자료가 꼬시래기류의 계통 및 진화를 이해하는데 유용함을 보여주고 있다.
꼬시래기는 우리나라 전연안(서해, 남해, 동해 및 제주)에 분포하는 주요 홍조류이며 유용성 자원생물로 활용가능성을 가지고 있다(Boo and Ko 2012). 우리나라를 포함한 북서태평양에 분포하는 꼬시래기의 분자마커 수준의 다양성 정보는 일부 가용하나 유전체 수준의 정보는 매우 미비하다. 따라서, 본 연구의 목적은 우리나라 꼬시래기의 색소체 및 미토콘드리아 유전체 자료를 확보하고 계통분류학적 유연관계를 명확히 파악하며, 유용성 해조류로써의 기초자료를 제공하는데 있다.
2. 재료 및 방법
실험대상인 꼬시래기는 전라남도 고흥군 소백일도 조간대(34˚41'37.82" N 127˚27'06.87" E)에서 2021년 5월 채집하였다(Fig. 1). 채집한 개체는 살아있는 상태로 실험실로 운반하였으며, 엽상체 일부는 건조표본으로 실리카겔과 함께 보관하였다. 일부 엽상체는 NGS (next-generation sequencing) 분석을 위해 15℃ 배양기(여과해수; L:D=14:10 조건)에 보관하면서 DNA 추출에 사용하였다.

Fig. 1
Collection locality and field sample images of Gracilaria vermiculophylla. (A) The specimen collected from Sobaekildo, Goheung, Jeonam (34.693842 N 127.451908 E) at 28 May 2021. (B) Field sample image of Gracilaria vermiculophylla.
배양기에 보관중인 꼬시래기 개체는 멸균한 여과해수를 사용하여 해부현미경하에서 부착생물을 제거하였다. 약 1 g의 생시료에 액체질소를 첨가하여 마쇄하고, NuclearBond AXG 100 with NucleoBond Buffer Set III (Macherey-Nalgel, Düren, Germany)를 사용하여 전체 DNA를 추출하였다. 추출한 전체 DNA의 순도 및 농도는 Qubit 3.0 Fluorometer와 Qubit dsDNA HS Assay Kit (Thermo Fisher Scientific Inc, Waltham, MA, USA) 그리고 NanoDrop One Spectrophotometers (Thermo Fisher Scientific Inc, Waltham, MA, USA)를 이용하여 측정하였다. 전장유전체시퀀싱(Whole Genome Sequencing)은 MGI Easy DNA Library Prep Kit와 MGISEQ-2000 (MGI Tech, Shenzhen, China)을 사용하는 시퀀싱 서비스(LAS, Gimpo, Korea)를 이용하였으며, 총 10 GB (Paired-end 101 bp read seqeunces)의 시퀀싱자료를 확보하였다.
꼬시래기 세포소기관(색소체 및 미토콘드리아) 유전체 어셈블리(genome assembly)는 NOVOPlasty V.4.3.1 (Dierckxsens et al. 2017)를 사용하였다. 색소체와 미토콘드리아 각각의 reference sequence (seed)는 NCBI GenBank MN853882 (Gracilaria vermiculophylla ptDNA, Li et al. 2020)과 NC_027064 (G. vermiculophylla mtDNA, Chi et al. Unpublished)을 사용하였다. 색소체 및 미토콘드리아 contigs의 완성도는 기존의 꼬시래기과 자료의 각 유전자 존재여부와 배열순서 비교를 통하여 판별하였다. 각 세포소기관 유전자의 annotation에는 다음과 같은 프로그램을 사용하였다, coding sequences (CDS): Geneious Prime V.2022.2.2 (http://www.geneious.com; Biomatters, Inc., Auckland, New Zealand), ribosomal RNA (rRNA): BLASTn (Altschul et al. 1990) 및 transfer RNA (tRNA): tRNAscan-SE V.2.0 (http://trna.ucsc.edu/tRNAscan-SE/; Chan et al. 2021). CDS 및 tRNA내 인트론은 reference sequence (NC_039092 G. vermiculophylla 색소체 유전체 및 MH396022 G. vermiculophylla 미토콘드리아 유전체, Iha et al. 2018)와 염기서열 유사도 99%를 기준으로 판단하였다.
꼬시래기류의 미토콘드리아 CDS 24개의 아미노산 서열은 Geneious Prime 프로그램의 translation alignment 옵션(hypothetical translation, transl_table 4)을 사용하여 정렬하였으며, 이후 alignment viewer를 이용하여 정렬상태를 직접 검토하였다. 계통수 구축에 사용한 유합 자료는 총 45개 분류군의 24개 CDS, 6,034 부위(positions)이다. 계통수 구축을 위한 각 유전자별 진화모델은 RAxML V.8.2.12의 ProteinModelSelection.pl 펄스크립을 이용하여 선택하였다(Stamatakis 2014). 유합자료의 최적 계통수는 RAxML V.8.2.12의 Maximum Likelhood (ML) 방법(-f a 옵션)을 이용하였으며 각 유전자별 아미노산 진화모델 및 GAMMA (rate heterogeneity)을 적용하였다(-q 옵션). 각 node의 단계통성은 1,000회의 bootstrap (-# 1000)으로 검증하였다. 최적의 ML 계통수 및 MLBt (ML bootstrap support value)는 FigTree V.4.4.4 (Rambaut 2009)를 이용하여 가시화하였다.
3. 결과 및 고찰
꼬시래기의 색소체 유전체(OP978508, complete 색소체 유전체, 평균 coverage 5,555X)는 총 180,269 bp 이다(Fig. 2). 전체 색소체 유전체는 35.2% A, 14.7% C, 14.7% G 및 29.5% T의 염기 함량으로 구성되어있다. 총 238개 유전자를 코딩하고 있으며 이는 204개 CDS, 3개 rRNA 및 30개 tRNA을 포함한다(Supplementary Table S1). 204개 CDS는 30개 ycf, 27개 rpl, 19개 rps, 18개 psb, 13개 orf, 11개 psa, 9개 pet, 8개 atp, 6개 apc, 4개 rpo, 각 3개의 acc, cpc 및 sec, 각 2개의 ccs, cpe, dna, ilv, inf, oda, rbc, suf, thi 및 trp, 그리고 각 1개의 arg, bas, car, cbb, cem, chl, clp, dfr, dsb, fab, ftr, fts, glt, gro, lys, moe, cbl, ctc, omp, pbs, pgm, pre, rne, rnz, tat, trx, tsf 및 tuf 유전자로 구성되어있다. 대부분(193개; 95%) CDS의 개시코돈은 ATG 이었으나, 일부 유전자는 TTG (chlI, gltB, ompR, orf292, trxA 및 ycf65) 또는 GTG (infC, petM, psaF, rbcS 및 rps8) 이다. 종결토돈은 TAA (155개 CDS; 76%), TAG (31개 CDS; 15%) 및 TGA (18개 CDS; 9%) 이다. 3개 rRNA는 각 1개의 rnl, rrn5 및 rns를 포함하며, 30개 tRNA는 각 3개의 trnL과 trnM, 각 2개의 trnG, trnS, trnT 및 trnV, 그리고 각 1개의 trnA, trnC, trnD, trnE, trnF, trnH, trnI, trnK, trnN, trnP, trnQ, trnW 및 trnY를 포함한다.
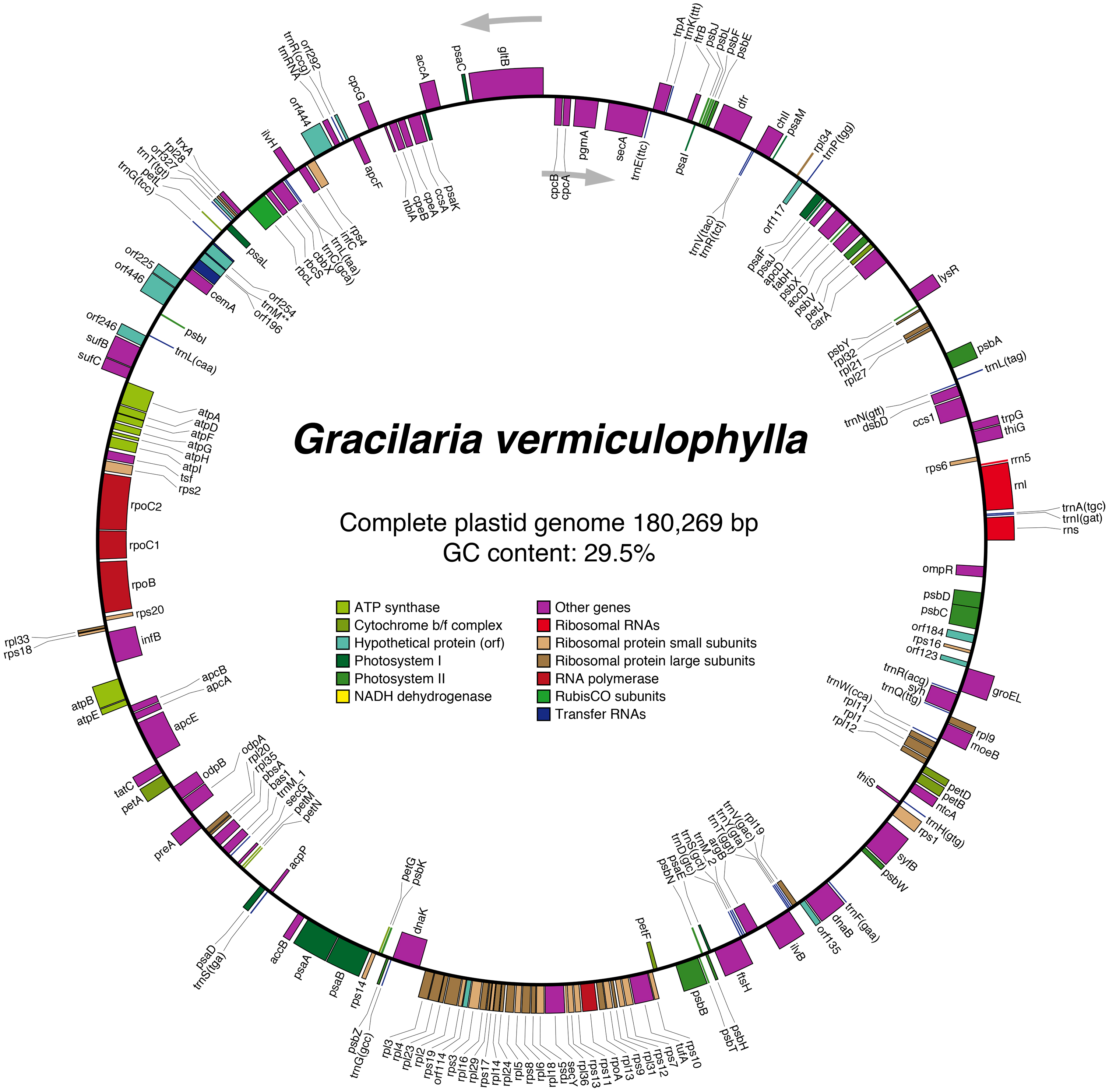
Fig. 2
Plastid genome map of Gracilaria vermiculophylla, 180,269 bp in total length. Genes on outside of circle are transcribed in counterclockwise direction and those on inside of circle are transcribed in clockwise direction. Colored boxes indicated functional gene categories shown in the circle.
고흥 꼬시래기의 색소체 유전체는 미국 및 중국 꼬시래기의 색소체 유전체와 거의 일치한다. GenBank에 있는 NC_039092 (G. vermiculophylla; 미국 버지니아 Hog Island, 10 Feb. 1999; Iha et al. 2018) 서열과 99.931% 일치하며, 변이 부위는 총 105 bp (0.069%)로 대부분 유전자 사이의 염기서열(intergenic sequence) 및 CDS내에 3번째 코돈(3rd codon position)에 위치한다. 고흥과 미국 Hog Island 개체간 4개의 삽입 및 결실(insertion-deletion; indel) 부위가 발견되었다. 고흥 개체 에서 3개의 삽입부위(rpoA-rpl13 유전자 사이 9 bp: AATATATTC, ycf46-psaM 유전자 사이 8 bp: TTTAGTTA, trpG-ccs1 유전자 사이 1 bp: A), Hog Island 개체에서 1개의 삽입부위(rps18-infB 유전자 사이 1 bp: T) 가 발견되었다. 중국 개체인 MN853882 (Qinhuangdao; Li et al. 2020)와는 99.934% 일치하며, 변이 부위는 총 110 bp (0.066%)이다. 고흥과 중국 Qinhuangdao 개체간 2개의 삽입 및 결실 부위가 발견되는데, 고흥 개체에서 8 bp (ycf46-psaM 유전자 사이: TTTAGTTA), Qinhuangdao 개체에서 1 bp (rps18-infB 유전자 사이: T) 삽입부위가 발견되었다.
한국-미국-중국 꼬시래기(G. vermiculophylla) 색소체 유전체는 높은 DNA 서열유사도(>99.9%)와 동일한 유전자 배열(synteny)을 보여주고 있다. 이는 꼬시래기과 세포소기관 유전체가 높은 보전성 을 갖는 다는 이전의 연구(Lyra et al. 2021)와 일치한다. 현재까지 알려진 꼬시래기과 8종의 종내 색소체 유전체는 DNA 서열 및 유전자 배열에서 매우 유사하며(종별 각 2개체: Gracilaria caudata MH396009와 MZ336047, G. chilensis MF401963과 MZ336051, G. crassissima MZ336054와 MZ336055, G. ferox MH396010과 MZ336058, G. rangiferina MH396012와 MZ336066, G. salinornia KF861575과 MZ336067, G. tikvahiae MZ336069와 MZ336070 및 Gracilariopsis longissima MH396014와 MZ336074), 그들의 단계통은 강하게 지지된다. 꼬시래기과의 색소체 유합(195개 CDS의 아미노산서열) ML계통수는 미토콘드리아 유합(24개 CDS의 아미노산서열) ML계통수와 동일한 계통관계를 보여주며, 이는 꼬시래기과의 형태진화[영양체 엽체모양(thallus shape), 웅성 배우체 정자낭 유형(spermatangial types), 과포자체 낭과 미세구조 등] 경향성과도 일치한다(Lyra et al. 2021). 따라서 꼬시래기과의 세포소기관 유전체는 종 이상의 형태적 진화 경향성 및 분류체계를 이해하는데 유용하다.
꼬시래기의 미토콘드리아 유전체(OP978509, partial 미토콘드리아 유전체, 평균 coverage 1,898X)는 총 26,090 bp 이다(Fig. 3). 전체 미토콘드리아 유전체의 염기 함량은 A: 37.6%, C: 13.9%, G: 14.5% 및 T: 34.0% 이다. 총 52개 유전자는 코딩부위는 25개 CDS, 3개 rRNA 및 24개 tRNA를 포함한다(Supplementary Table S2). 25개 CDS는 7개 nad, 4개 atp, 각 3개의 cox, rps 및 sdh, 2개의 rpl, 그리고 각 1개의 cob, orf, tat 유전자로 구성되어있다. 다수(21개; 87.5%)의 CDS 개시코돈은 ATG 이었으며 2개 유전자(atp6 및 cox2)는 TTG, 그리고 rpl20는 ATT 이다. 종결코돈은 TAA (22개 CDS; 88%) 및 TAG (atp8, nad4 및 rpl16; 12%) 이다. 3개 rRNA는 각 1개의 rnl, rrn5 및 rns를 포함하며, 24개 tRNA는 각 2개의 trnG, trnL, trnM, trnR 및 trnS, 그리고 각 1개의 trnA, trnC, trnD, trnE, trnF, trnH, trnI, trnK, trnN, trnP, trnQ, trnV, trnW 및 trnY를 포함한다.
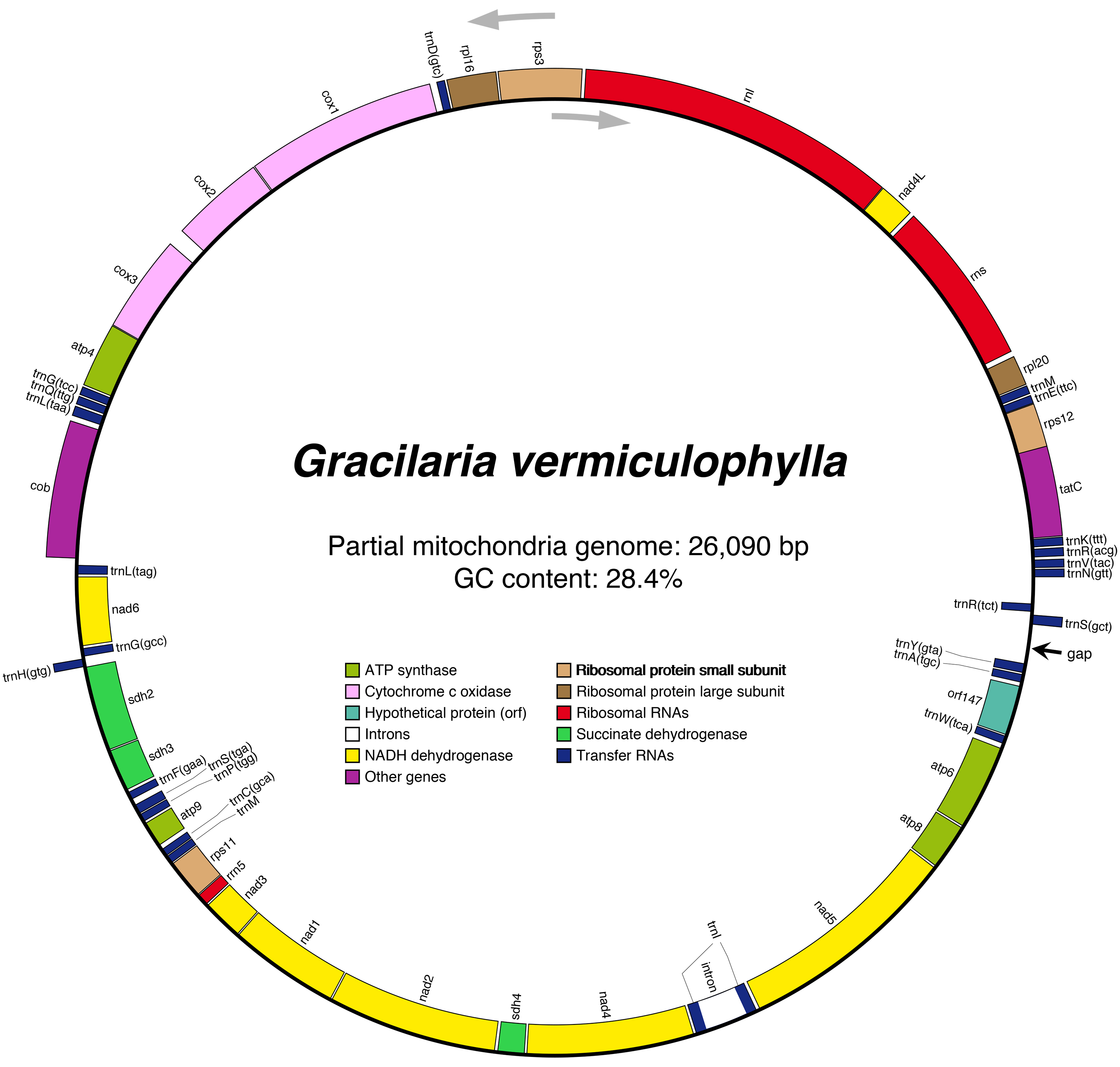
Fig. 3
Mitochondria genome map of Gracilaria vermiculophylla, 26,090 bp in total length. Genes on outside of circle are transcribed in counterclockwise direction and those on inside of circle are transcribed in clockwise direction. Colored boxes indicated functional gene categories shown in the circle. Arrow indicates an unfilled gap between trnS and trnY.
고흥 꼬시래기의 미토콘드리아 유전체는 미국 및 중국 꼬시래기의 미토콘드리아 유전체와 거의 일치한다. 염기서열 유사도는 MH396022 (미국 버지니아 Hog Island, 10 Feb. 1999; Iha et al. 2018)와 99.52%, NC_027064 (중국 voucher 201103102; Chi et al. Unpublished)와 94.78% 그리고 KJ526627 (중국 voucher 201104055; Chi et al. Unpublished)와 94.16%이다. 미토콘드리아 24개 CDS 아미노산서열 유합계통수는 이를 잘 반영하고 있다(Fig. 4). 꼬시래기 4개체의 계통관계를 반영한 미토콘드리아 유전체 정렬 결과에서는 총 15개 삽입 및 결실부위를 발견하였다. (#1) 3 bp (GGC) 삽입부위는 고흥 꼬시래기의 rps16-trnD 유전자 사이 서열부분 에서만 발견된다. (#2) atp9-trnC 유전자 사이의 1 bp 삽입은 고흥과 중국(voucher 201104055, KJ526627) 재료가 공유하고 있다. 꼬시래기 4개체의 미토콘드리아 유전체 정렬에서 발견된 총 15개의 삽입 및 결실 부위 중 9개(#3-#11)가 nad3-nad1-nad2-sdh4-nad4 (총 4,894 bp)에 집중되어있다. (#3) nad3-nad1 유전자 사이의 1 bp 삽입은 중국 개체(voucher 201104055, KJ526627)에서만 발견되었으며, (#4) nad1-nad2 유전자 사이의 6 bp 결실은 고흥과 미국 Hog Island 개체가 공유한다. (#5, #6) nad2 유전자내 2개의 결실(3 bp와 6 bp)은 중국의 2개체에서만 발견되었다. (#7) nad2-sdh4 유전자 사이 15 bp 삽입, (#8) sdh4-nad4 유전자 사이 9 bp 삽입, (#12) atp6-trnW 유전자 사이 26 bp 삽입, (#14) trnY-trnN 유전자 사이 386 bp 삽입(trnS와 trnR 포함)은 고흥과 미국 Hog Island 개체가 공유한다. (#13) trnY-trnS 유전자 사이 1 bp와 (#15) trnS-trnN 유전자 사이 62 bp 결실은 고흥의 개체에서만 발견되었다. 중국의 2개체만 발견된 nad4-인트론 (#9) 및 2개의 결실 (#10, #11) 부위는 추가적인 검증이 필요한 변이로 추정된다. 꼬시래기 4개체(고흥, 미국 및 중국 2개체) 비교시, nad3-nad1-nad2-sdh4-nad4 (총 4,894 bp) 부위는 9개의 삽입 및 결실 부위를 포함하며, 염기서열 유사도는 78% 이하이다. 이는 이전의 꼬시래기 연구에서 쓰인 cox1 유전자를 포함하는 cox1-cox2-cox3-atp4-cob 부위(총 5,333 bp 유사도 99.8%)와 비교시, 보다 더 많은 변이가 집중되어 있다. 따라서 nad3-nad1-nad2-sdh4-nad4부위는 꼬시래기의 개체군 생태 및 생물지리학적 연구에 좀 더 높은 활용가능성을 보여준다.
Fig. 4
Phylogeny and partial mitochondria genome alignment (from nad3 to trnR) of Gracilaria vermiculophylla. The maximum likelihood (ML) tree was construed based on 24 concatenated mitochondrial protein sequences, total 6,034 positions. The monophyly of each node are indicated by number near node which tested by using 1,000 bootstrap replications (MLBt). On the top, multiple genome alignment of four G. vermiculophylla. DNA indels among taxa are indicated by dot lines with numbers (#3-15).
꼬시래기과의 미토콘드리아 아미노산서열 유합자료(24개 CDS의 아미노산 총 6,034 부위) ML계통수(Fig. 4)는 꼬시래기류 종 및 속간 관계를 보여주고 있으며, 최근의 유전체 분석결과(Lyra et al. 2021)와 일치한다. 우리나라 고흥, 미국 Hog Island, 및 중국(2개체)의 꼬시래기(G. vermiculophylla)의 단계통은 강하게 지지된다(100% MLBt; Fig. 4). 꼬시래기와 G. tenuistipitat - G. chilensis clade는 근연관계에 있다(93% MLBt). 미토콘드리아 유합 계통수는 꼬시래기속(Gracilaria; 100% MLBt)과 개꼬시래기속(Gracilariopsis; 100% MLBt) 각각의 단계통성, Melathalia속의 기저부 위치(96% MLBt), 그리고 꼬시래기과(Gracilariaceae)의 단계통성을 잘 보여준다. 우리나라에 분포하는 꼬시래기과 중 가용한 세포소기관 유전체 자료는 개꼬시래기(Gracilariopsis chorda; Yang et al. 2014; Lee et al. 2016)가 유일하다. 본 연구결과는 우리나라 꼬시래기속 홍조류 종의 첫번째 세포소기관 유전체 정보 및 계통수를 제공한다. 우리나라를 포함한 북서태평양 또는 전세계에 분포하는 유용성 꼬시래기류[예, 꼬불꼬시래기(G. incurvata), 각시꼬시래기(G. parvispora) 및 잎꼬시래기(G. textorii) 등]의 명확한 계통관계 파악 및 유전적 다양성 정보의 확대를 위해 추가적인 세포소기관 유전체 자료의 확보 및 분석이 필요하다.
4. 결론
본 연구에서는 우리나라 고흥에 분포하는 꼬시래기(Gracilaria vermiculophylla)의 색소체(180,269 bp, 29.5% GC)와 미토콘드리아(26,090 bp, 28.4% GC)의 유전체 자료를 분석하였다. 이전에 알려진 미국 및 중국 꼬시래기 개체와 비교를 통하여, 색소체 유전체는 각 유전자의 존재 여부 및 배열순서에서 매우 유사함(99.9% 유사도)을 확인하였다. 미토콘드리아 유전체에서는 유전자 존재여부에서 차이(한국과 미국개체에 trnS와 trnR 추가 존재)와 함께 종내 개체군 연구에 적합한 높은 변이 부위(nad3-nad1-nad2-sdh4-nad4, 유사도 78%)를 발견하였다. 미토콘드리아 유전체 유합계통수는 우리나라 고흥의 개체가 중국보다 미국 Hog Island 개체와 유사함을 보여준다. 새로운 세포소기관 유전체 자료는 유용성 꼬시래기류의 다양성 및 계통연구에 중요한 기초자료가 될 것이다.
Supplementary
Supplementary Table S1.
Gracilaria vermiculophylla : 3 plastid genome annotation.
|
Type
|
#
|
Name
| |
ptDNA
|
|
GenBank accession no.
Product
|
OP978508
Korea
Length
(bp)
|
NC_039092
USA
Length
(bp)
|
MN853882
China
Length
(bp)
|
|
CDS
|
1
|
accA CDS
|
acetyl-CoA carboxylase, carboxyl transferase subunit alpha
|
972
|
972
|
972
|
|
2
|
accB CDS
|
acetyl-CoA carboxylase, biotin carboxyl carrier protein
|
501
|
501
|
501
|
|
3
|
accD CDS
|
acetyl-CoA carboxylase, carboxyl transferase subunit beta
|
867
|
867
|
867
|
|
4
|
acpP CDS
|
acyl carrier protein
|
264
|
264
|
264
|
|
5
|
apcA CDS
|
allophycocyanin alpha subunit
|
486
|
486
|
486
|
|
6
|
apcB CDS
|
allophycocyanin beta subunit
|
486
|
486
|
486
|
|
7
|
apcD CDS
|
allophycocyanin gamma subunit
|
486
|
486
|
486
|
|
8
|
apcE CDS
|
phycobilisome linker polypeptide
|
2,643
|
2,643
|
2,643
|
|
9
|
apcF CDS
|
allophycocyanin beta 18 subunit
|
510
|
510
|
510
|
|
10
|
argB CDS
|
acetylglutamate kinase
|
858
|
858
|
858
|
|
11
|
atpA CDS
|
ATP synthase CF1 subunit alpha
|
1,512
|
1,512
|
1,512
|
|
12
|
atpB CDS
|
ATP synthase CF1 subunit beta
|
1,422
|
1,422
|
1,422
|
|
13
|
atpD CDS
|
ATP synthase CF1 subunit delta
|
558
|
558
|
558
|
|
14
|
atpE CDS
|
ATP synthase CF1 subunit epsilon
|
405
|
405
|
405
|
|
15
|
atpF CDS
|
ATP synthase CF0 subunit I
|
516
|
516
|
516
|
|
16
|
atpG CDS
|
ATP synthase CF0 subunit II
|
477
|
477
|
477
|
|
17
|
atpH CDS
|
ATP synthase CF0 subunit III
|
249
|
249
|
249
|
|
18
|
atpI CDS
|
ATP synthase CF0 subunit IV
|
747
|
747
|
747
|
|
19
|
bas1 CDS
|
2-Cys peroxiredoxin
|
600
|
600
|
600
|
|
20
|
carA CDS
|
carbamoyl phosphate synthase small subunit
|
1,188
|
1,188
|
1,188
|
|
21
|
cbbX CDS
|
Rubisco expression protein
|
876
|
876
|
876
|
|
22
|
ccs1 CDS
|
Cytochrome c biogenesis protein
|
1,317
|
1,317
|
1,317
|
|
23
|
ccsA CDS
|
heme attachment to plastid cytochrome c
|
861
|
861
|
861
|
|
24
|
cemA CDS
|
envelope membrane protein
|
837
|
837
|
837
|
|
25
|
chlI CDS
|
Mg chelatase subunit e
|
1,071
|
1,071
|
1,071
|
|
26
|
clpC CDS
|
Clp protease ATP binding subunit
|
2,469
|
2,469
|
2,469
|
|
27
|
cpcA CDS
|
phycocyanin alpha subunit
|
489
|
489
|
489
|
|
28
|
cpcB CDS
|
phycocyanin beta subunit
|
519
|
519
|
519
|
|
29
|
cpcG CDS
|
phycobilisome rod-core linker polypeptide
|
702
|
702
|
702
|
|
30
|
cpeA CDS
|
phycoerythrin subunit a
|
495
|
495
|
495
|
|
31
|
cpeB CDS
|
phycoerythrin subunit b
|
534
|
534
|
534
|
|
32
|
dfr CDS
|
drug sensory protein A
|
1,908
|
1,908
|
1,908
|
|
33
|
dnaB CDS
|
replication helicase subunit
|
1,782
|
1,782
|
1,782
|
|
34
|
dnaK CDS
|
Hsp70-type chaperone
|
1,866
|
1,866
|
1,866
|
|
35
|
dsbD CDS
|
thiol:disulfide interchange protein
|
711
|
711
|
711
|
|
36
|
fabH CDS
|
beta-ketoacyl-acyl carrier protein synthase III
|
993
|
993
|
993
|
|
37
|
ftrB CDS
|
ferredoxin thioreductase subunit b
|
351
|
351
|
351
|
|
38
|
ftsH CDS
|
cell division protein FTSH
|
1,881
|
1,881
|
1,881
|
|
39
|
gltB CDS
|
glutamate synthase
|
4,584
|
4,584
|
4,584
|
|
40
|
groEL CDS
|
60-kDa chaperonin
|
1,587
|
1,587
|
1,587
|
|
41
|
ilvB CDS
|
acetohydroxyacid synthetase large subunit
|
1,797
|
1,797
|
1,797
|
|
42
|
ilvH CDS
|
acetohydroxyacid synthetase small subunit
|
528
|
528
|
528
|
|
43
|
infB CDS
|
translation initiation factor 2
|
2,076
|
2,076
|
2,076
|
|
44
|
infC CDS
|
translation initiation factor 3
|
546
|
546
|
546
|
|
45
|
lysR CDS
|
lysR transcriptional regulator
|
930
|
930
|
930
|
|
46
|
moeB CDS
|
molybdopterin biosynthesis protein
|
1,065
|
1,065
|
1,065
|
|
47
|
nblA CDS
|
phycobilisome degradation protein
|
174
|
174
|
174
|
|
48
|
ntcA CDS
|
global nitrogen transcriptional regulator
|
654
|
654
|
654
|
|
49
|
odpA CDS
|
pyruvate dehydrogenase E1 component alpha subunit
|
1,026
|
1,026
|
1,026
|
|
50
|
odpB CDS
|
pyruvate dehydrogenase E1 component beta subunit
|
972
|
972
|
972
|
|
51
|
ompR CDS
|
putative transcriptional regulator ompR
|
729
|
729
|
729
|
|
52
|
orf114 CDS
|
hypothetical protein
|
345
|
345
|
345
|
|
53
|
orf117 CDS
|
hypothetical protein
|
354
|
354
|
354
|
|
54
|
orf123 CDS
|
hypothetical protein
|
372
|
372
|
372
|
|
55
|
orf135 CDS
|
hypothetical protein
|
408
|
408
|
408
|
|
56
|
orf184 CDS
|
hypothetical protein
|
555
|
555
|
555
|
|
57
|
orf196 CDS
|
hypothetical protein
|
591
|
591
|
591
|
|
58
|
orf225 CDS
|
hypothetical protein
|
678
|
678
|
678
|
|
59
|
orf246 CDS
|
hypothetical protein
|
741
|
741
|
741
|
|
60
|
orf254 CDS
|
hypothetical protein
|
765
|
765
|
765
|
|
61
|
orf292 CDS
|
hypothetical protein
|
225
|
225
|
225
|
|
62
|
orf327 CDS
|
hypothetical protein
|
219
|
219
|
219
|
|
63
|
orf444 CDS
|
hypothetical protein
|
1,335
|
1,335
|
1,335
|
|
64
|
orf446 CDS
|
hypothetical protein
|
1,341
|
1,341
|
1,341
|
|
65
|
pbsA CDS
|
heme oxygenase
|
696
|
696
|
696
|
|
66
|
petA CDS
|
apocytochrome f
|
933
|
933
|
933
|
|
67
|
petB CDS
|
cytochrome b6
|
648
|
648
|
648
|
|
68
|
petD CDS
|
cytochrome b6/f complex subunit 4
|
483
|
483
|
483
|
|
69
|
petF CDS
|
ferredoxin
|
300
|
300
|
300
|
|
70
|
petG CDS
|
cytochrome b6/f complex subunit 5
|
114
|
114
|
114
|
|
71
|
petJ CDS
|
cytochrome c553
|
327
|
327
|
327
|
|
72
|
petL CDS
|
cytochrome b6-f complex subunit 6
|
96
|
96
|
96
|
|
73
|
petM CDS
|
cytochrome b6-f complex subunit 7
|
99
|
99
|
99
|
|
74
|
petN CDS
|
cytochrome b6-f complex subunit 8
|
93
|
93
|
93
|
|
75
|
pgmA CDS
|
phosphoglycerate mutase
|
1,536
|
1,536
|
1,536
|
|
76
|
preA CDS
|
prenyl transferase
|
972
|
972
|
972
|
|
77
|
psaA CDS
|
photosystem I P700 apoprotein A1
|
2,259
|
2,259
|
2,259
|
|
78
|
psaB CDS
|
photosystem I P700 apoprotein A2
|
2,205
|
2,205
|
2,205
|
|
79
|
psaC CDS
|
photosystem I subunit VII (iron-sulfur center)
|
246
|
246
|
246
|
|
80
|
psaD CDS
|
photosystem I reaction center subunit II
|
426
|
426
|
426
|
|
81
|
psaE CDS
|
photosystem I reaction center subunit IV
|
186
|
186
|
186
|
|
82
|
psaF CDS
|
photosystem I reaction center subunit III
|
558
|
558
|
558
|
|
83
|
psaI CDS
|
photosystem I reaction center subunit VIII
|
111
|
111
|
111
|
|
84
|
psaJ CDS
|
photosystem I reaction center subunit IX
|
129
|
129
|
129
|
|
85
|
psaK CDS
|
photosystem I reaction center subunit X
|
261
|
261
|
261
|
|
86
|
psaL CDS
|
photosystem I reaction center subunit XI
|
453
|
453
|
453
|
|
87
|
psaM CDS
|
photosystem I reaction center subunit M
|
93
|
93
|
93
|
|
88
|
psbA CDS
|
photosystem II reaction center protein D1
|
1,083
|
1,083
|
1,083
|
|
89
|
psbB CDS
|
photosystem II CP47 chlorophyll apoprotein
|
1,530
|
1,530
|
1,530
|
|
90
|
psbC CDS
|
photosystem II CP43 chlorophyll apoprotein
|
1,461
|
1,461
|
1,461
|
|
91
|
psbD CDS
|
photosystem II reaction center protein D2
|
1,056
|
1,056
|
1,056
|
|
92
|
psbE CDS
|
photosystem II cytochrome b559 alpha subunit
|
255
|
255
|
255
|
|
93
|
psbF CDS
|
photosystem II cytochrome b559 beta subunit
|
135
|
135
|
135
|
|
94
|
psbH CDS
|
photosystem II 10 kDa phosphoprotein
|
204
|
204
|
204
|
|
95
|
psbI CDS
|
photosystem II protein I
|
117
|
117
|
117
|
|
96
|
psbJ CDS
|
photosystem II protein J
|
120
|
120
|
120
|
|
97
|
psbK CDS
|
photosystem II protein K
|
138
|
138
|
138
|
|
98
|
psbL CDS
|
photosystem II protein L
|
117
|
117
|
117
|
|
99
|
psbN CDS
|
photosystem II protein N
|
132
|
132
|
132
|
|
100
|
psbT CDS
|
photosystem II protein T
|
96
|
96
|
96
|
|
101
|
psbV CDS
|
photosystem II cytochrome c550
|
495
|
495
|
495
|
|
102
|
psbW CDS
|
photosystem II protein psb28
|
345
|
345
|
345
|
|
103
|
psbX CDS
|
photosystem II protein X
|
120
|
120
|
120
|
|
104
|
psbY CDS
|
photosystem II protein Y
|
105
|
105
|
105
|
|
105
|
psbZ CDS
|
photosystem II protein Z
|
189
|
189
|
189
|
|
106
|
rbcL CDS
|
ribulose-1,5-bisphosphate carboxylase/oxygenase large subunit
|
1,467
|
1,467
|
1,467
|
|
107
|
rbcS CDS
|
ribulose-1,5-bisphosphate carboxylase/oxygenase small subunit
|
417
|
417
|
417
|
|
108
|
rne CDS
|
ribonuclease E
|
1,491
|
1,491
|
1,491
|
|
109
|
rnz CDS
|
ribonuclease Z
|
681
|
681
|
681
|
|
110
|
rpl1 CDS
|
ribosomal protein L1
|
705
|
705
|
705
|
|
111
|
rpl11 CDS
|
ribosomal protein L11
|
426
|
426
|
426
|
|
112
|
rpl12 CDS
|
ribosomal protein L12
|
396
|
396
|
396
|
|
113
|
rpl13 CDS
|
ribosomal protein L13
|
432
|
432
|
432
|
|
114
|
rpl14 CDS
|
ribosomal protein L14
|
369
|
369
|
369
|
|
115
|
rpl16 CDS
|
ribosomal protein L16
|
408
|
408
|
408
|
|
116
|
rpl18 CDS
|
ribosomal protein L18
|
318
|
318
|
318
|
|
117
|
rpl19 CDS
|
ribosomal protein L19
|
369
|
369
|
369
|
|
118
|
rpl2 CDS
|
ribosomal protein L2
|
828
|
828
|
828
|
|
119
|
rpl20 CDS
|
ribosomal protein L20
|
354
|
354
|
354
|
|
120
|
rpl21 CDS
|
ribosomal protein L21
|
324
|
324
|
324
|
|
121
|
rpl23 CDS
|
ribosomal protein L23
|
306
|
306
|
306
|
|
122
|
rpl24 CDS
|
ribosomal protein L24
|
255
|
255
|
255
|
|
123
|
rpl27 CDS
|
ribosomal protein L27
|
255
|
255
|
255
|
|
124
|
rpl28 CDS
|
ribosomal protein L28
|
195
|
195
|
195
|
|
125
|
rpl29 CDS
|
ribosomal protein L29
|
201
|
201
|
201
|
|
126
|
rpl3 CDS
|
ribosomal protein L3
|
621
|
621
|
621
|
|
127
|
rpl31 CDS
|
ribosomal protein L31
|
228
|
228
|
228
|
|
128
|
rpl32 CDS
|
ribosomal protein L32
|
171
|
171
|
171
|
|
129
|
rpl33 CDS
|
ribosomal protein L33
|
198
|
198
|
198
|
|
130
|
rpl34 CDS
|
ribosomal protein L34
|
138
|
138
|
138
|
|
131
|
rpl35 CDS
|
ribosomal protein L35
|
201
|
201
|
201
|
|
132
|
rpl36 CDS
|
ribosomal protein L36
|
114
|
114
|
114
|
|
133
|
rpl4 CDS
|
ribosomal protein L4
|
654
|
654
|
654
|
|
134
|
rpl5 CDS
|
ribosomal protein L5
|
540
|
540
|
540
|
|
135
|
rpl6 CDS
|
ribosomal protein L6
|
546
|
546
|
546
|
|
136
|
rpl9 CDS
|
ribosomal protein L9
|
465
|
465
|
465
|
|
137
|
rpoA CDS
|
RNA polymerase subunit alpha
|
945
|
945
|
945
|
|
138
|
rpoB CDS
|
RNA polymerase subunit beta
|
3,360
|
3,360
|
3,360
|
|
139
|
rpoC1 CDS
|
RNA polymerase b'-subunit
|
1,887
|
1,887
|
1,887
|
|
140
|
rpoC2 CDS
|
RNA polymerase b''-subunit
|
3,690
|
3,690
|
3,690
|
|
141
|
rps1 CDS
|
ribosomal protein S1
|
798
|
798
|
798
|
|
142
|
rps10 CDS
|
ribosomal protein S10
|
318
|
318
|
318
|
|
143
|
rps11 CDS
|
ribosomal protein S11
|
390
|
390
|
390
|
|
144
|
rps12 CDS
|
ribosomal protein S12
|
375
|
375
|
375
|
|
145
|
rps13 CDS
|
ribosomal protein S13
|
381
|
381
|
381
|
|
146
|
rps14 CDS
|
ribosomal protein S14
|
303
|
303
|
303
|
|
147
|
rps16 CDS
|
ribosomal protein S16
|
240
|
240
|
240
|
|
148
|
rps17 CDS
|
ribosomal protein S17
|
243
|
243
|
243
|
|
149
|
rps18 CDS
|
ribosomal protein S18
|
213
|
213
|
213
|
|
150
|
rps19 CDS
|
ribosomal protein S19
|
279
|
279
|
279
|
|
151
|
rps2 CDS
|
ribosomal protein S2
|
696
|
696
|
696
|
|
152
|
rps20 CDS
|
ribosomal protein S20
|
294
|
294
|
294
|
|
153
|
rps3 CDS
|
ribosomal protein S3
|
654
|
654
|
654
|
|
154
|
rps4 CDS
|
ribosomal protein S4
|
606
|
606
|
606
|
|
155
|
rps5 CDS
|
ribosomal protein S5
|
519
|
519
|
519
|
|
156
|
rps6 CDS
|
ribosomal protein S6
|
312
|
312
|
312
|
|
157
|
rps7 CDS
|
ribosomal protein S7
|
471
|
471
|
471
|
|
158
|
rps8 CDS
|
ribosomal protein S8
|
399
|
399
|
399
|
|
159
|
rps9 CDS
|
ribosomal protein S9
|
414
|
414
|
414
|
|
160
|
secA CDS
|
preprotein-translocase subunit a
|
2,649
|
2,649
|
2,649
|
|
161
|
secG CDS
|
Preprotein translocase SecG subunit
|
216
|
216
|
216
|
|
162
|
secY CDS
|
SecY-type transporter protein
|
1,236
|
1,236
|
1,236
|
|
163
|
sufB CDS
|
sufB protein
|
1,431
|
1,431
|
1,431
|
|
164
|
sufC CDS
|
Iron-sulfur cluster formation ABC transporter ATP-binding subunit
|
771
|
771
|
771
|
|
165
|
syfB CDS
|
phenylalanine-tRNA ligase beta subunit
|
2,109
|
2,109
|
2,109
|
|
166
|
syh CDS
|
histidine-tRNA ligase
|
1,233
|
1,233
|
1,233
|
|
167
|
tatC CDS
|
Sec-independent protein translocase component TatC
|
717
|
717
|
717
|
|
168
|
thiG CDS
|
Thiamine biosynthesis protein G
|
831
|
831
|
831
|
|
169
|
thiS CDS
|
Thiamine biosynthesis protein
|
216
|
216
|
216
|
|
170
|
trpA CDS
|
tryptophan synthase alpha subunit
|
807
|
807
|
807
|
|
171
|
trpG CDS
|
anthranilate synthase component II
|
567
|
567
|
567
|
|
172
|
trxA CDS
|
thioredoxin
|
333
|
333
|
333
|
|
173
|
tsf CDS
|
translation elongation factor Ts
|
606
|
606
|
606
|
|
174
|
tufA CDS
|
translation elongation factor Tu
|
1,230
|
1,230
|
1,230
|
|
175
|
ycf12 CDS
|
hypothetical protein
|
105
|
105
|
105
|
|
176
|
ycf17 CDS
|
hypothetical protein
|
159
|
159
|
159
|
|
177
|
ycf19 CDS
|
hypothetical protein
|
291
|
291
|
291
|
|
178
|
ycf20 CDS
|
hypothetical protein
|
276
|
276
|
276
|
|
179
|
ycf21 CDS
|
hypothetical protein
|
537
|
537
|
537
|
|
180
|
ycf22 CDS
|
hypothetical protein
|
468
|
468
|
468
|
|
181
|
ycf23 CDS
|
hypothetical protein
|
738
|
738
|
738
|
|
182
|
ycf29 CDS
|
hypothetical protein
|
654
|
654
|
654
|
|
183
|
ycf3 CDS
|
photosystem I assembly protein ycf3
|
513
|
513
|
513
|
|
184
|
ycf33 CDS
|
hypothetical protein
|
198
|
198
|
198
|
|
185
|
ycf34 CDS
|
hypothetical protein
|
228
|
228
|
228
|
|
186
|
ycf35 CDS
|
hypothetical protein
|
390
|
390
|
390
|
|
187
|
ycf36 CDS
|
hypothetical protein
|
504
|
504
|
504
|
|
188
|
ycf38 CDS
|
ABC transporter
|
888
|
888
|
888
|
|
189
|
ycf39 CDS
|
hypothetical protein
|
972
|
972
|
972
|
|
190
|
ycf4 CDS
|
photosystem I assembly protein ycf4
|
552
|
552
|
552
|
|
191
|
ycf41 CDS
|
hypothetical protein
|
306
|
306
|
306
|
|
192
|
ycf45 CDS
|
hypothetical protein
|
1,689
|
1,689
|
1,689
|
|
193
|
ycf46 CDS
|
hypothetical protein
|
1,476
|
1,476
|
1,476
|
|
194
|
ycf52 CDS
|
hypothetical protein
|
546
|
546
|
546
|
|
195
|
ycf53 CDS
|
hypothetical protein
|
732
|
732
|
732
|
|
196
|
ycf54 CDS
|
hypothetical protein
|
315
|
315
|
315
|
|
197
|
ycf55 CDS
|
hypothetical protein
|
975
|
975
|
975
|
|
198
|
ycf58 CDS
|
hypothetical protein
|
462
|
462
|
462
|
|
199
|
ycf59 CDS
|
Mg-protoporphyrin IX monomethyl ester oxidative cyclase
|
1,050
|
1,050
|
1,050
|
|
200
|
ycf60 CDS
|
hypothetical protein
|
615
|
615
|
615
|
|
201
|
ycf61 CDS
|
DNA-directed RNA polymerase omega chain
|
222
|
222
|
222
|
|
202
|
ycf62 CDS
|
tRNAIle-lysidine synthetase
|
960
|
960
|
960
|
|
203
|
ycf63 CDS
|
hypothetical protein
|
723
|
723
|
723
|
|
204
|
ycf65 CDS
|
plastid-specific 30S ribosomal protein 3
|
300
|
300
|
300
|
|
ncRNA
|
1
|
rnpB ncRNA
|
ribonuclease P RNA
|
369
|
369
|
369
|
|
rRNA
|
1
|
rnl rRNA
|
large subunit ribosomal RNA
|
2,871
|
2,871
|
2,871
|
|
2
|
rns rRNA
|
small subunit ribosomal RNA
|
1,487
|
1,487
|
1,487
|
|
3
|
rrn5 rRNA
|
5S ribosomal RNA
|
118
|
118
|
118
|
|
tRNA
|
1
|
trnA(tgc) tRNA
|
tRNA-Ala
|
73
|
73
|
73
|
|
2
|
trnC(gca) tRNA
|
tRNA-Cys
|
71
|
71
|
71
|
|
3
|
trnD(gtc) tRNA
|
tRNA-Asp
|
74
|
74
|
74
|
|
4
|
trnE(ttc) tRNA
|
tRNA-Glu
|
73
|
73
|
73
|
|
5
|
trnF(gaa) tRNA
|
tRNA-Phe
|
73
|
73
|
73
|
|
6
|
trnG(gcc) tRNA
|
tRNA-Gly
|
72
|
72
|
72
|
|
7
|
trnG(tcc) tRNA
|
tRNA-Gly
|
71
|
71
|
71
|
|
8
|
trnH(gtg) tRNA
|
tRNA-His
|
74
|
74
|
74
|
|
9
|
trnI(gat) tRNA
|
tRNA-Ile
|
74
|
74
|
74
|
|
10
|
trnK(ttt) tRNA
|
tRNA-Lys
|
72
|
72
|
72
|
|
11
|
trnL(caa) tRNA
|
tRNA-Leu
|
83
|
83
|
83
|
|
12
|
trnL(taa) tRNA
|
tRNA-Leu
|
85
|
85
|
85
|
|
13
|
trnL(tag) tRNA
|
tRNA-Leu
|
83
|
83
|
83
|
|
14
|
trnM tRNA
|
tRNA-Met
|
87
|
87
|
87
|
|
15
|
trnM 1 tRNA
|
tRNA-Met
|
74
|
74
|
74
|
|
16
|
trnM 2 tRNA
|
tRNA-Met
|
74
|
74
|
74
|
|
17
|
trnN(gtt) tRNA
|
tRNA-Asn
|
72
|
72
|
72
|
|
18
|
trnP(tgg) tRNA
|
tRNA-Pro
|
74
|
74
|
74
|
|
19
|
trnQ(ttg) tRNA
|
tRNA-Gln
|
72
|
72
|
72
|
|
20
|
trnR(acg) tRNA
|
tRNA-Arg
|
74
|
74
|
74
|
|
21
|
trnR(ccg) tRNA
|
tRNA-Arg
|
73
|
73
|
73
|
|
22
|
trnR(tct) tRNA
|
tRNA-Arg
|
73
|
73
|
73
|
|
23
|
trnS(gct) tRNA
|
tRNA-Ser
|
90
|
90
|
90
|
|
24
|
trnS(tga) tRNA
|
tRNA-Ser
|
86
|
86
|
86
|
|
25
|
trnT(ggt) tRNA
|
tRNA-Thr
|
72
|
72
|
72
|
|
26
|
trnT(tgt) tRNA
|
tRNA-Thr
|
73
|
73
|
73
|
|
27
|
trnV(gac) tRNA
|
tRNA-Val
|
74
|
74
|
74
|
|
28
|
trnV(tac) tRNA
|
tRNA-Val
|
72
|
72
|
72
|
|
29
|
trnW(cca) tRNA
|
tRNA-Trp
|
73
|
73
|
73
|
|
30
|
trnY(gta) tRNA
|
tRNA-Tyr
|
82
|
82
|
82
|
Supplementary Table S2.
Gracilaria vermiculophylla : 4 mitochondria genome annotation.
|
Type
|
#
|
Name
| |
mtDNA
|
|
GenBank accession no.
product
|
OP978509
Korea
Length
(bp)
|
MH396022
USA
Length
(bp)
|
NC_027064
China 1
Length
(bp)
|
KJ526627
China 2
Length
(bp)
|
|
CDS
|
1
|
atp4 CDS
|
ATP synthase F0 subunit b
|
543
|
543
|
543
|
543
|
|
2
|
atp6 CDS
|
ATP synthase F0 subunit a
|
759
|
759
|
759
|
759
|
|
3
|
atp8 CDS
|
ATP synthase F0 subunit 8
|
408
|
408
|
408
|
408
|
|
4
|
atp9 CDS
|
ATP synthase F0 subunit c
|
231
|
231
|
231
|
231
|
|
5
|
cob CDS
|
apocytochrome b
|
1,140
|
1,140
|
1,140
|
1,140
|
|
6
|
cox1 CDS
|
cytochrome c oxidase subunit 1
|
1,596
|
1,596
|
1,596
|
1,596
|
|
7
|
cox2 CDS
|
cytochrome c oxidase subunit 2
|
789
|
789
|
792
|
792
|
|
8
|
cox3 CDS
|
cytochrome c oxidase subunit 3
|
819
|
819
|
819
|
819
|
|
9
|
nad1 CDS
|
NADH dehydrogenase subunit 1
|
981
|
981
|
981
|
981
|
|
10
|
nad2 CDS
|
NADH dehydrogenase subunit 2
|
1,497
|
1,497
|
1,476
|
1,476
|
|
11
|
nad3 CDS
|
NADH dehydrogenase subunit 3
|
366
|
366
|
366
|
366
|
|
12
|
nad4 CDS
|
NADH dehydrogenase subunit 4
|
1,476
|
1,476
|
1,461
|
1,461
|
|
13
|
nad4L CDS
|
NADH dehydrogenase subunit 4L
|
306
|
306
|
306
|
306
|
|
14
|
nad5 CDS
|
NADH dehydrogenase subunit 5
|
1,977
|
1,977
|
1,977
|
1,977
|
|
15
|
nad6 CDS
|
NADH dehydrogenase subunit 6
|
609
|
609
|
609
|
609
|
|
16
|
orf147 CDS
|
hypothetical protein
|
444
|
444
|
444
|
444
|
|
17
|
rpl16 CDS
|
ribosomal protein L16
|
414
|
414
|
414
|
414
|
|
18
|
rpl20 CDS
|
ribosomal protein L20
|
255
|
255
|
234
|
234
|
|
19
|
rps11 CDS
|
ribosomal protein S11
|
354
|
354
|
354
|
354
|
|
20
|
rps12 CDS
|
ribosomal protein S12
|
369
|
369
|
369
|
369
|
|
21
|
rps3 CDS
|
ribosomal protein S3
|
696
|
696
|
696
|
696
|
|
22
|
sdh2 CDS
|
succinate dehydrogenase subunit 2
|
753
|
753
|
753
|
753
|
|
23
|
sdh3 CDS
|
succinate dehydrogenase subunit 3
|
375
|
375
|
375
|
375
|
|
24
|
sdh4 CDS
|
succinate dehydrogenase subunit 4
|
240
|
240
|
240
|
240
|
|
25
|
tatC CDS
|
Sec-independent protein translocase component TatC
|
768
|
768
|
768
|
768
|
|
rRNA
|
1
|
rnl rRNA
|
large subunit ribosomal RNA
|
2,655
|
2,655
|
2,636
|
2,636
|
|
2
|
rns rRNA
|
small subunit ribosomal RNA
|
1,375
|
1,375
|
1,397
|
1,397
|
|
3
|
rrn5 rRNA
|
5S ribosomal RNA
|
107
|
107
|
107
|
107
|
|
tRNA
|
1
|
trnA(tgc)
|
tRNA-Ala
|
75
|
75
|
75
|
75
|
|
2
|
trnC(gca) tRNA
|
tRNA-Cys
|
72
|
72
|
72
|
72
|
|
3
|
trnD(gtc) tRNA
|
tRNA-Asp
|
72
|
72
|
72
|
72
|
|
4
|
trnE(ttc) tRNA
|
tRNA-Glu
|
73
|
73
|
73
|
73
|
|
5
|
trnF(gaa) tRNA
|
tRNA-Phe
|
73
|
73
|
73
|
73
|
|
6
|
trnG(gcc) tRNA
|
tRNA-Gly
|
74
|
74
|
74
|
74
|
|
7
|
trnG(tcc) tRNA
|
tRNA-Gly
|
74
|
74
|
74
|
74
|
|
8
|
trnH(gtg) tRNA
|
tRNA-His
|
75
|
75
|
74
|
74
|
|
9
|
trnI tRNA
|
tRNA-Ile
|
73
|
73
|
73
|
73
|
|
tRNA-intron
|
trnI intron
| |
494
|
494
|
494
|
494
|
|
10
|
trnK(ttt) tRNA
|
tRNA-Lys
|
74
|
74
|
74
|
74
|
|
11
|
trnL(taa) tRNA
|
tRNA-Leu
|
86
|
86
|
86
|
86
|
|
12
|
trnL(tag) tRNA
|
tRNA-Leu
|
84
|
84
|
84
|
84
|
|
13
|
trnM tRNA
|
tRNA-Met
|
75
|
75
|
75
|
75
|
|
14
|
trnM tRNA
|
tRNA-Met
|
74
|
74
|
74
|
74
|
|
15
|
trnN(gtt) tRNA
|
tRNA-Asn
|
72
|
72
|
72
|
72
|
|
16
|
trnP(tgg) tRNA
|
tRNA-Pro
|
74
|
74
|
74
|
74
|
|
17
|
trnQ(ttg) tRNA
|
tRNA-Gln
|
73
|
73
|
73
|
73
|
|
18
|
trnR(acg) tRNA
|
tRNA-Arg
|
75
|
75
|
75
|
75
|
|
19
|
trnR(tct) tRNA
|
tRNA-Arg
|
73
|
73
|
-
|
-
|
|
20
|
trnS(gct) tRNA
|
tRNA-Ser
|
87
|
87
|
-
|
-
|
|
21
|
trnS(tga) tRNA
|
tRNA-Ser
|
88
|
88
|
88
|
88
|
|
22
|
trnV(tac) tRNA
|
tRNA-Val
|
73
|
73
|
73
|
73
|
|
23
|
trnW(tca) tRNA
|
tRNA-Trp
|
74
|
74
|
74
|
74
|
|
24
|
trnY(gta) tRNA
|
tRNA-Tyr
|
86
|
86
|
86
|
86
|